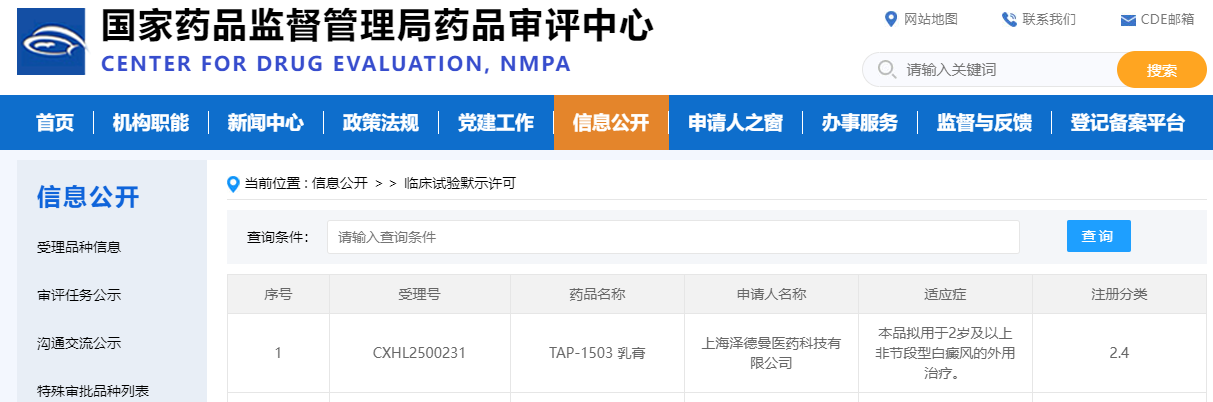
近日,由上海澤德曼醫(yī)藥科技有限公司自主研發(fā)的外用芳香烴受體(AhR)調(diào)節(jié)劑藥品正式獲得國(guó)家藥品監(jiān)督管理局藥品審評(píng)中心(CDE)批準(zhǔn),即將開(kāi)展治療白癜風(fēng)的確證性臨床試驗(yàn),。這一突破標(biāo)志著我國(guó)甚至世界范圍內(nèi)在皮膚疾病創(chuàng)新藥物研發(fā)領(lǐng)域邁出重要一步,。
中國(guó)醫(yī)科大學(xué)附屬第一醫(yī)院皮膚科教授、中華醫(yī)學(xué)會(huì)皮膚性病學(xué)分會(huì)主任委員高興華介紹:“白癜風(fēng)作為一種常見(jiàn)的皮膚疾病,,全球患者數(shù)量已達(dá)4000萬(wàn)至8000萬(wàn),,其中我國(guó)患者約700萬(wàn)。長(zhǎng)期以來(lái),,臨床治療面臨重大挑戰(zhàn),,急需新藥、好藥,?!睋?jù)了解,全球范圍內(nèi)僅有美國(guó)FDA批準(zhǔn)的一款外用藥物,,而我國(guó)臨床仍主要依賴20多年前的老藥,。
據(jù)介紹,本款AhR調(diào)節(jié)劑藥物通過(guò)全新作用機(jī)制,,展現(xiàn)三大治療優(yōu)勢(shì):精準(zhǔn)調(diào)控免疫系統(tǒng)異常反應(yīng),,有效保護(hù)黑色素細(xì)胞功能,促進(jìn)黑色素再生,。這一創(chuàng)新療法不僅解決了傳統(tǒng)藥物治療效果有限的問(wèn)題,,其良好的安全性更使其特別適合長(zhǎng)期治療需求。
臨床數(shù)據(jù)顯示,,約90%的白癜風(fēng)患者曾遭受不同程度歧視,,患者抑郁風(fēng)險(xiǎn)更是高達(dá)普通人群的5倍。北京大學(xué)人民醫(yī)院皮膚科教授張建中表示:“這款創(chuàng)新藥物一旦研發(fā)成功,,有望為患者帶來(lái)全新的治療選擇和更好的生活質(zhì)量保障,。”
此次臨床試驗(yàn)的開(kāi)展,,將為這一創(chuàng)新療法的安全性和有效性提供科學(xué)依據(jù),。業(yè)內(nèi)普遍認(rèn)為,這不僅是我國(guó)在皮膚疾病治療領(lǐng)域的重要突破,,更是全球范圍內(nèi)白癜風(fēng)治療的一次革命性進(jìn)展,。未來(lái)若通過(guò)臨床驗(yàn)證,將成為改寫(xiě)白癜風(fēng)治療格局的重要里程碑,。